2024年6月14日,我院李伟广研究员团队联合国家儿童医学中心(上海)儿童脑科学中心、上海交通大学医学院附属上海儿童医学中心麻醉科与儿科临床药理学实验室张马忠主任医师团队,以及上海交通大学医学院附属瑞金医院罗艳主任团队,在《Communications Biology》上发表了题为《An ultra-short-acting benzodiazepine in thalamic nucleus reuniens undermines fear extinction via intermediation of hippocamposeptal circuits》的研究论文。该研究基于苯二氮䓬类麻醉剂瑞马唑仑(remimazolam)的快速起效和短时持续特性,系统地阐释了苯二氮䓬类药物在恐惧消退神经环路中的作用机制。研究发现,苯二氮䓬类药物作为常见抗焦虑治疗,虽然能够有效缓解焦虑症状,但同时也会干扰恐惧消退的过程。这一发现为解决苯二氮䓬类药物抗焦虑治疗与基于恐惧消退理论的临床暴露疗法在治疗焦虑症和创伤后应激障碍(PTSD)中的矛盾提供了新的科学依据。

在现代社会,焦虑症是一种常见的心理健康问题。苯二氮䓬类药物作为常见的抗焦虑制剂,被广泛用于治疗。恐惧消退作为一种抑制性学习和记忆,帮助机体适应变化的环境,是基于行为认知疗法纠正焦虑症和创伤后应激障碍(PTSD)等情感精神障碍的理论基础。苯二氮䓬类药物与基于恐惧消退的暴露疗法联合使用时,基础和临床研究提示其可能对恐惧消退和安全信号识别产生负面影响。恐惧消退训练期间暴露于苯二氮䓬类药物会导致机体产生特定的内感受情景(一种药物服用后的特定内感受状态),消退记忆提取测试阶段的药物缺失则通过导致(内感受)情景变换诱发已消退恐惧记忆的重现(fear renewal)。此外,苯二氮䓬类药物还可能通过降低条件性恐惧反应水平,进而破坏机体对抗条件性恐惧反应必需的新学习所依赖的预测误差。事实上,关于苯二氮䓬类药物对于恐惧消退的影响还往往被其伴随的镇静、催眠和麻醉等药理作用所干扰,因此有必要使用一种超短效苯二氮䓬类药物来区分其对恐惧消退的影响,同时尽量减少对内感受状态的干扰。
瑞马唑仑是一种新型苯二氮䓬类麻醉剂,具有更快的起效时间、更短的镇静持续时间和更快的恢复速度。在这项最新研究中,李伟广研究员团队与合作者一起,通过使用瑞马唑仑,旨在探讨苯二氮䓬类药物对恐惧消退的影响及其背后的神经环路机制。恐惧消退依赖于包括腹侧海马(ventral hippocampus, vHPC)、内侧前额叶皮层(mPFC)和基底外侧杏仁核(BLA)在内的三元环路的交互参与。此外,丘脑连接核(thalamic nucleus reuniens, RE)不仅向vHPC发出密集投射,还从mPFC接收密集投射,因此在恐惧消退过程中发挥着连接mPFC和vHPC功能的关键作用。
研究人员首先明确了瑞马唑仑在不影响运动活性的前提下对恐惧消退产生影响的剂量范围。全脑免疫组化染色实验评估了活动诱导的即刻早期基因c-fos的表达,表明瑞马唑仑处理组在丘脑连接核(RE)和腹侧海马(vHPC)中的神经元活性显著降低,而在外侧隔区(lateral septum, LS)中的神经元活性则显著增加,表明瑞马唑仑重新配置了恐惧消退相关脑区的神经元活动。
在丘脑连接核(RE)定点给予瑞马唑仑可产生类似全身给药的阻碍恐惧消退的作用。电生理学实验表明,瑞马唑仑作为苯二氮䓬类制剂通过增强GABA(A)受体活性进而促进丘脑连接核(RE)的GABA能突触传递,并降低RE神经元的兴奋性。利用工具病毒介导的、在丘脑连接核(RE)针对GABA(A)受体γ2亚基的选择性基因敲减,可取消瑞马唑仑对恐惧消退的调控作用。通过神经环路特异的GABA(A)受体γ2亚基基因敲减后回补实验,研究人员发现,瑞马唑仑依赖于选择性向vHPC发出神经投射的丘脑连接核(RE)神经元(即RE-vHPC投射神经元)来实现恐惧消退调控作用。进一步研究还发现,瑞马唑仑通过增强外侧隔区(LS)向丘脑连接核(RE)的长程GABA能突触传递阻断恐惧消退。光遗传学激活LS向RE的神经投射,可产生类似瑞马唑仑的损害恐惧消退的效应。
最后,研究人员基于丘脑连接核(RE)与腹侧海马(vHPC)之间的神经投射,外侧隔区(LS)与丘脑连接核(RE)之间的长距离GABA能投射,以及已知的腹侧海马(vHPC)与外侧隔区(LS)之间的神经投射,刻画了这几个脑区围成的一条正反馈促恐惧消退的神经环路(图1):丘脑连接核(RE)向腹侧海马(vHPC)发送单突触兴奋性神经投射,而腹侧海马则向外侧隔区(LS)的GABA能神经元发送前馈抑制性神经投射,后者与从外侧隔区(LS)到丘脑连接核(RE)的长距离GABA能神经投射相结合,形成了一条正反馈神经环路。丘脑连接核(RE)特异性的瑞马唑仑通过破坏这一环路,进而削弱恐惧消退过程。
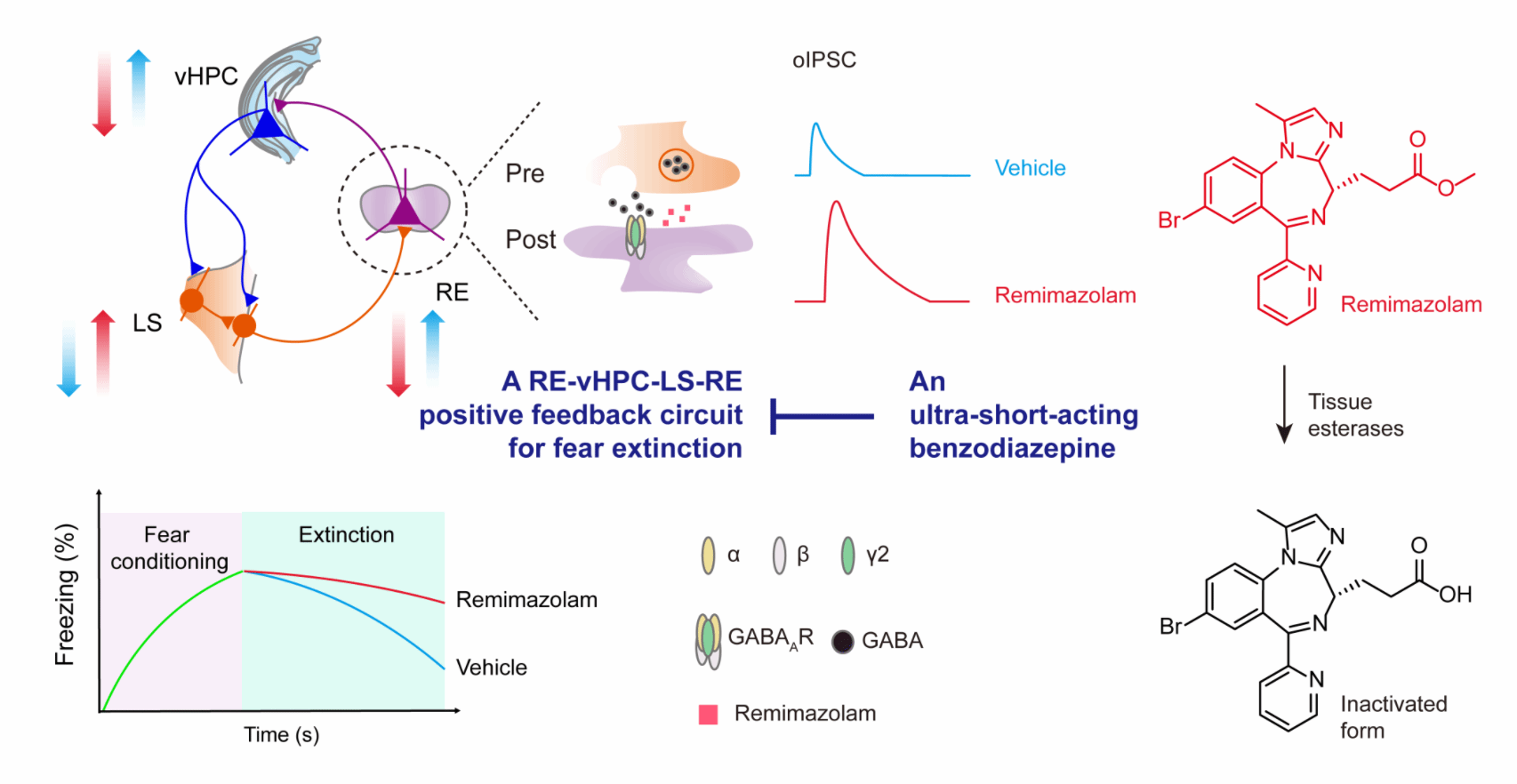
图1. 瑞马唑仑通过调控RE→vHPC→LS→RE环路损害恐惧消退的神经机制。
总之,该研究不仅阐明了苯二氮䓬类药物通过调控特定神经环路影响恐惧消退的机制,还为临床上苯二氮䓬类药物与基于消退的暴露疗法的结合使用提供了新的理论基础,有望为焦虑症和PTSD等精神疾病的治疗带来全新的启发。
国家儿童医学中心(上海)儿童脑科学中心、上海交通大学医学院附属上海儿童医学中心麻醉科已毕业博士、上海交通大学医学院附属瑞金医院张海燕博士,与我院余同舟硕士研究生和易昕博士后为该论文的共同第一作者。我院李伟广研究员,上海交通大学医学院附属上海儿童医学中心副院长、麻醉科学科带头人、上海儿童医学中心贵州医院院长张马忠教授,上海交通大学医学院附属瑞金医院麻醉科罗艳主任为该论文的共同通讯作者。
该研究得到了科技创新2030-“脑科学与类脑研究”重大项目、国家自然科学基金、上海市等各级项目的支持。该研究还得到了上海交通大学医学院徐天乐教授、上海交通大学医学院附属上海儿童医学中心麻醉科郑吉建主任等的合作支持。
论文链接:https://www.nature.com/articles/s42003-024-06417-w